KÁRI & UPPLÝSTA SAMÞYKKIÐ

„Myrkur leikur um lífsýni og gögn sem aflað er í faraldrinum, enginn veit hvert þau fara, á grundvelli hvaða heimilda þeirra er aflað, til hvers þau verða notuð og þau virðast hvorki afturkallanleg né notkun þeirra kæranleg. Stjórnvöld og rannsóknarstofnanir eru í Villta Vestrinu,“ segir Haukur Arnþórsson stjórnsýslufræðingur í nýrri grein á Vísir.is.
Í greininni er óheftur aðgangur ÍE að lífsýnum í gegnum skimanir fyrir COVID-19 gagnrýndur og þá umfram allt leynd sem hvíli yfir meðferð gagnanna. Hvert fara lífsýnin okkar? spyr Haukur og segir:
„DeCode – sem þjóðin hafnaði að gefa lífssýni fyrir nokkrum misserum – safnar nú lífsýnum þjóðarinnar sem aldrei fyrr. Fyrirtækið er í eigu Amgen líftæknifyrirtækisins í Kaliforníu, sem segist nota getu og uppgötvanir DeCode til eigin rannsókna og lyfjaframleiðslu. Við erum líklega að gefa bandarísku stórfyrirtæki dýrmætustu upplýsingar um okkur sem við getum gefið um þessar mundir. Fyrr eða síðar getur það kallað til sín eignir sínar á Íslandi og flutt starfsemina milli landa.“
Haukur segir að þær skimanir sem ÍE er að framkvæma núna séu gerðar án samþykkis vísindasiðanefndar og þær virðist undanþegnar almennum skilyrðum stjórnvalda fyrir vinnslunni. Óttast Haukur að ÍE hafi frítt spil varðandi meðferð á lífsýnunum.
Haukur telur ljóst að skimanirnar muni standa yfir í langan tíma en enginn viti hvað lífsýnin verða varðveitt lengi eða til hvaða hluta þau verði notuð. „Lífsýni eru dýrmætasta eign okkar nú á dögum og má nota þau í margháttuðum tilgangi á markaði, við kúganir, í stjórnmálum og opinberu lífi – og til flokkunar þjóðfélagsþegnanna af öllu tagi. Annars er það bara hugmyndaflugið sem takmarkar notkunarmöguleika lífsýna í dag,“ segir Haukur.
Í upplýsingatækni sé gögnum aldrei eytt, ávallt reyni þeir sem hafa þau undir höndum að hagnýta sér þau eins mikið og kostur er.
„Það segir sig sjálft að myrkur leikur um þessa vinnslu, almenningi er ekki sagt hvað verði um lífsýnin eða veittar allar upplýsingar um hvert þau fara, til hvers þau verða notuð o.s.frv. og þá ekki um rétt sinn,“ segir Haukur.
Haukur telur að kórónuveirufaraldurinn muni standa í tvö til tvö og hálft ár. Hann spyr hvort réttlætanlegrt sé að leggja grundvallarmannréttindi fólks til hliðar í svo langan tíma, jafnvel þó að verið sé að glíma við illvígan faraldur. Hann spyr hvort viðbrögðin séu hættulegri en tilefnið.

Þá fjallar Kári um eign bandaríska félagsins Amgen á Íslenskri erfðagreiningu, en Haukur gerði að því skóna að uppgötvanir ÍE nýttust því fyrst og fremst bandarísku lyfjafyrirtæki frekar en almenningi.
Kári svarar: Íslensk erfðagreining birtir allar uppgötvanir sem eru gerðar í fyrirtækinu eins hratt og mögulegt er þannig að þær eru öllum lyfjafyrirtækjum aðgengilegar til þess að nýta, ekki bara Amgen. Við höfum oft sagt þetta opinberlega og þar með er það partur af upplýstu samþykkjunum sem þátttakendur skrifa undir. Það er hins vegar hagur sjúklinga að það sé í það minnsta eitt lyfjafyrirtæki sem vilji eyða í það orku að skoða uppgötvanir um sjúkdóma þeirra með það í huga að búa til lyf. Það er ekki alltaf sjálfgefið að svo sé.
Þá benti Kári enn og aftur á það að ÍE á ekki gagnasafn sem það hefur í vörslu sinni, heldur sé það eign íslensku þjóðarinnar. Segir Kári ekki geta gefið það sem það á ekki.
Kári gaf svo ekki mikið fyrir staðhæfingar Hauks um að rannsóknir ÍE væru án samþykkir vísindasiðanefndar: „Það er nokkuð ljóst á þessari staðhæfingu Hauks að hann hefur tekið sér fasta búsetu út í mýri.“ Sagði Kári að öll sýni, stroka úr nefholi og munni, væru hent í ruslið eftir að búið væri að leita að veirunni og eftir atvikum, raðgreina veiruna.
Kári lýkur máli svo á að benda á að ásakanir Hauks séu alvarlegar, svo alvarlegar raunar að Kári útilokar ekki að hann verði látinn bera ábyrgð á þeim orðum fyrir dómstólum.
Alma Möller landlæknir: Ekki verður krafist upplýsts samþykkis fyrir bólusetningunni.

Umsókn um klíníska lyfjarannsókn á mönnum þarf að fara fyrir Lyfjastofnun, Vísindasiðanefnd og Persónuvernd – Engin umsókn hafði borist frá Pfizer þremur mánuðum eftir að C-19 bólusetningar hófust á Íslandi og finnst hvergi.
Klínísk lyfjarannsókn – Umsókn um klíníska lyfjarannsókn á mönnum þarf að fara fyrir Lyfjastofnun, Vísindasiðanefnd og Persónuvernd.
Það þarf líka að að gefa upp sé aðalrannsakandi lyfjarannsóknarinnar er og hver sé ábyrgðaraðili sem er í þessu tilfelli Lyfjastofnunog þá undir eftirliti Landlæknis.
Þá á rannsóknin að vera aðgengileg almenningi á heimasíðu lyfjastofnunarinnar en það er hún ekki.
UPPLÝST SAMÞYKKI
25. Þátttaka einstaklinga sem færir eru um að veita upplýst samþykki fyrir þátttöku í læknisfræðilegri rannsókn, skal vera af frjálsum vilja.
- Þótt viðeigandi geti verið að ráðgast við aðra í fjölskyldunni og forsvarsmenn samfélagsins, má ekki skrá neinn sem fær er um að veita upplýst samþykki til þátttöku í rannsókn, nema viðkomandi veiti samþykki sitt af frjálsum vilja.
https://gudrunbergmann.is/gengid-a-mannrettindin
26.
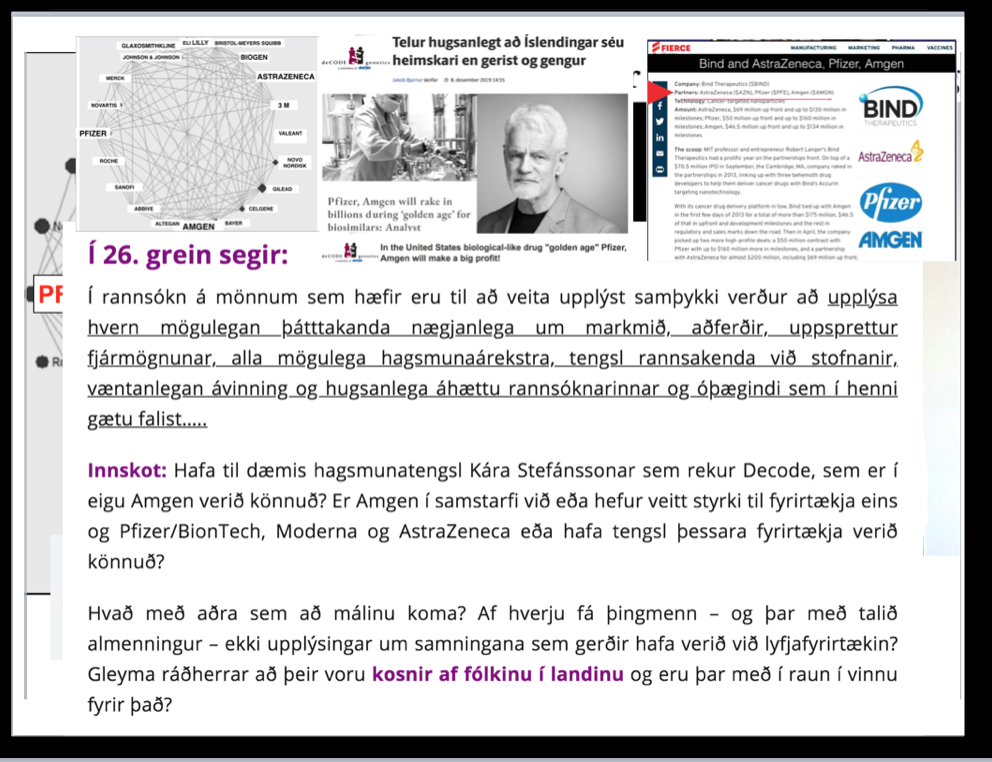
Í rannsókn á mönnum sem hæfir eru til að veita upplýst samþykki verður að upplýsa hvern mögulegan þátttakanda nægjanlega um markmið, aðferðir, uppsprettur fjármögnunar, alla mögulega hagsmunaárekstra,tengsl rannsakanda við stofnanir, væntanlegan ávinning og hugsanlega áhættu rannsóknarinnar og óþægindi, sem í henni gætu falist, hvaða ráðstafanir eru ráðgerðar þegar rannsókn er lokið og öll önnur atriði varðandi rannsóknina sem gætu skipt máli.
- Mögulegan þátttakanda verður að upplýsa um réttinn til neita að taka þátt í rannsókninni eða að draga samþykki sitt til baka hvenær sem er, án eftirmála.
- Sérstaka athygli skal veita upplýsingaþörfum hvers og eins mögulegs þátttakanda, svo og því hvaða aðferðum er beitt til þess að koma upplýsingunum til skila.
- Eftir að hafa fullvissað sig um það, að mögulegur þátttakandi hafi skilið upplýsingarnar, skal læknirinn eða annar hæfur einstaklingur leita upplýsts samþykkis mögulega þátttakandans, sem veitt er af frjálsum vilja, helst skriflega. Ef ekki er unnt að afla skriflegs samþykkis, verður að skjalfesta og vottfesta formlega hið óskrifaða samþykki.
- Allir þátttakendur í rannsókn skulu eiga þess kost að fá upplýsingar um almenna útkomu og niðurstöður rannsóknarinnar.
27.
- Þegar leitað er upplýsts samþykkis fyrir þátttöku í rannsóknarverkefni, skal læknirinn vera sérlega varkár, ef mögulegur þátttakandinn er háður honum eða gæti veitt samþykki sitt nauðugur.
- Í slíkum tilvikum skal annar hæfur einstaklingur sem er algerlega óháður þessu sambandi leita upplýsts samþykkis.
28.
- Ef mögulegur þátttakandi í rannsókn er ekki fær um að veita upplýst samþykki, verður rannsakandinnað leita upplýsts samþykkis lögráðamanns.
- Slíka einstaklinga má ekki að taka inn sem þátttakendur ef engar líkur eru á að rannsóknin verði þeim sjálfum til ávinnings, nema því aðeins að rannsóknin sé ætluð til þess að efla heilbrigði þess hóps, sem mögulegur þátttakandi tilheyrir, að ekki sé í staðinn hægt að gera þessa rannsókn á einstaklingum sem færir eru um að veita upplýst samþykki og að rannsóknin feli aðeins í sér lágmarks áhættu og léttustu byrði.
29.
- Þegar mögulegur þátttakandi, sem telst ófær um að veita upplýst samþykki, er fær um að veita jáyrði sitt við ákvörðunum um þátttöku í rannsókn verður rannsakandinn að leita þess jáyrðis, auk samþykkis lögráðamannsins.
- Beri mögulegur þátttakandi fram andmæli skal virða þau.
30.
- Rannsókn á einstaklingum sem eru líkamlega eða andlega ófærir um að veita samþykki, svo sem meðvitundarlausum sjúklingum, má því aðeins gera, að það andlega eða líkamlega ástand sem kemur í veg fyrir að upplýsta samþykkisins sé veitt, sé nauðsynlegt sérkenni rannsóknarþýðisins.
- Við slíkar aðstæður skal læknirinn leita upplýsts samþykkis lögráðamanns.
- Sé enginn slíkur lögráðamaður tiltækur og þoli rannsóknin enga bið, má rannsóknin hefjast án upplýsts samþykkis, að því tilskildu, að þeim sértæku ástæðum fyrir því að þátttakendur í því ástandi,sem gerir þeim ókleift að veita upplýst samþykki, sé lýst í rannsóknaráætlun og að rannsóknin hafi verið samþykkt af vísindasiðanefnd.
- Samþykkis fyrir áframhaldandi þátttöku ætti að afla svo fljótt sem kostur er frá einstaklingnum eða lögráðamanni hans.
31.
- Læknirinn verður að upplýsa sjúklinginn um það að fullu, hvaða þáttur í umönnun hans tengist rannsókninni.
- Neiti sjúklingur að taka þátt í rannsókn eða ákveði að draga sig út úr henni, má það aldrei hafa neikvæð áhrif á samband sjúklings og læknis.
32.
- Fyrir læknisfræðilegar rannsóknir þar sem notaðar eru persónugreinanlegar upplýsingar eða efni úr mönnum, t.d. rannsóknir á efni eða upplýsingum úr lífsýnasafni eða svipuðum söfnum, verða læknar að leita upplýsts samþykkis fyrir söfnun, varðveislu og/eða endurnotkun þeirra.
- Þó geta einkar óvenjulegar aðstæður gert að verkum að ómögulegt eða illframkvæmanlegt er að afla samþykkis fyrir slíkri rannsókn.
- Við slíkar aðstæður má aðeins gera rannsóknina eftir umfjöllun og samþykki vísindasiðanefndar.

https://www.lyfjastofnun.is/frettir/sidasti-dagur-til-ad-senda-inn-umsokn-um-kliniska-lyfjarannsokn-a-arinu-2017-er-15-desember-2017/
Um höfund

- ✞༺(((( Ⓒilla ℜągnąℜṧ )))༻♚༺ BA Classical Art Historian || MA Culture & Media || Tourism & Sales Management || Web Design || Photo & Videographer for Tourism Magasins ༻
Síðustu færslur
 MANNRÉTTINDI19. nóvember, 2024MENNTASPJALL VALGERÐAR SNÆLAND JÓNSDÓTTUR
MANNRÉTTINDI19. nóvember, 2024MENNTASPJALL VALGERÐAR SNÆLAND JÓNSDÓTTUR Sigurlaug Ragnarsdóttir15. ágúst, 2024‘Really Chilling’: Five Countries to Test European Vaccination Card
Sigurlaug Ragnarsdóttir15. ágúst, 2024‘Really Chilling’: Five Countries to Test European Vaccination Card MANNRÉTTINDI9. ágúst, 2024Lög um borgaralega handtöku voru felld úr gildi árið 2008
MANNRÉTTINDI9. ágúst, 2024Lög um borgaralega handtöku voru felld úr gildi árið 2008 Óflokkað30. maí, 2024GLÚMUR SEGIR ARNAR ÞÓR VERA MEÐ VITLAUSAR SKOÐANIR
Óflokkað30. maí, 2024GLÚMUR SEGIR ARNAR ÞÓR VERA MEÐ VITLAUSAR SKOÐANIR