Í fylgiseðlingum á bls 30 eru eftirfarandi kaflar:

Upplýsingar um Comirnaty og við hverju það er notað
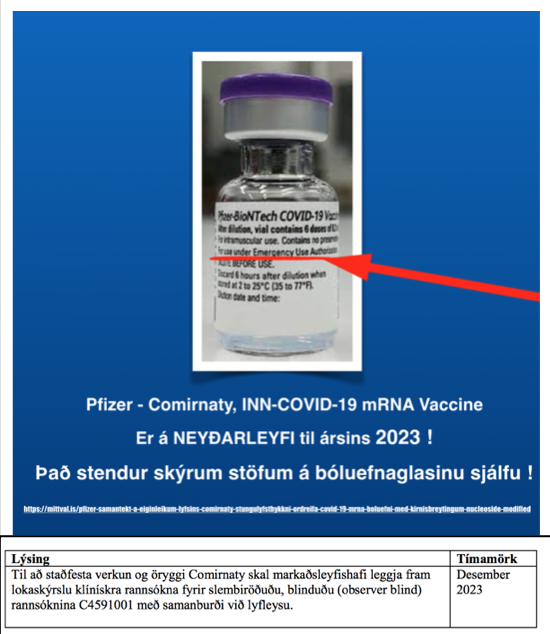
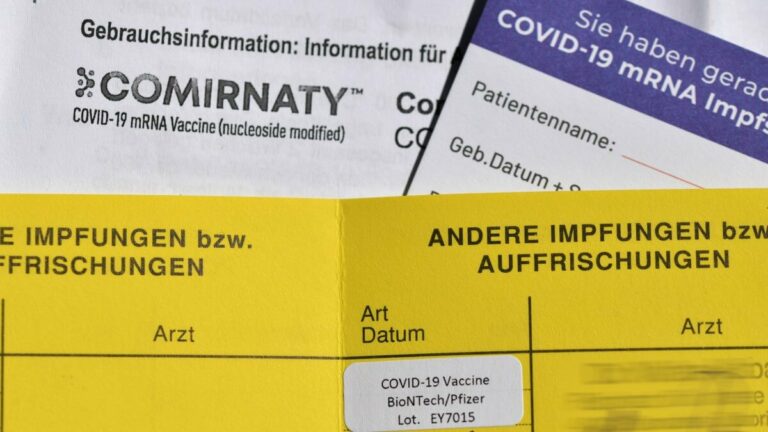
Comirnaty er bóluefni sem notað er til að koma í veg fyrir COVID-19 af völdum SARS-CoV-2 veiru.
- Comirnaty er gefið fullorðnum og unglingum, 12 ára og eldri.
- Bóluefnið fær ónæmiskerfið (náttúrulegar varnir líkamans) til að framleiða mótefni og blóðfrumur sem vinna gegn veirunni og veitir þannig vörn gegn COVID-19.
- Þú getur ekki fengið COVID-19 af Comirnaty af því að það inniheldur ekki veiru til myndunar ónæmis.
Áður en þú færð Comirnaty – Varnaðarorð og varúðarreglur. Eins og við á um öll bóluefni, þá er ekki víst að 2 skammta bólusetningin með Comirnaty veiti öllum sem hana fá fulla vörn og ekki er þekkt hversu lengi vörnin varir.
Kafli 4.2 – 4.6
Bls 3 – 5
BÖRN
Ekki hefur enn verið sýnt fram á öryggi og verkun Comirnaty hjá börnum yngri en 12 ára.
Takmarkaðar upplýsingar liggja fyrir.
Gefa má einstaklingum 18 ára og eldri örvunarskammt (þriðja skammtinn) af Comirnaty að minnsta kosti 6 mánuðum eftir annan skammtinn.
MEÐGANGA
Kafli 4.6 – bls 5
Frjósemi, Meðganga og Brjóstagjöf
- Takmörkuð reynsla liggur fyrir af notkun Comirnaty á meðgöngu.
- Dýrarannsóknir benda hvorki til beinna né óbeinna skaðlegra áhrifa á meðgöngu, þroska fósturvísis/fósturs, fæðingu eða þroska eftir fæðingu (sjá kafla 5.3).
- Aðeins skal íhuga gjöf Comirnaty á meðgöngu ef hugsanlegir kostir vega þyngra en hugsanleg áhætta fyrir móður og fóstur.
Brjóstagjöf.
- Ekki er þekkt hvort Comirnaty skilst út í brjóstamjólk.
Frjósemi Dýrarannsóknir benda hvorki til beinna né óbeinna skaðlegra áhrifa á æxlun (sjá kafla 5.3).
VIÐAUKI II bls, 22 – 23
E. Sérstök skylda til að ljúka aðgerðum eftir útgáfu Neyðarleyfis sbr. skilyrts markaðsleyfis. Þetta lyf hefur fengið markaðsleyfi með skilyrtu samþykki og í samræmi við grein 14-a í reglugerð (EB) nr. 726/2004 skal markaðsleyfishafi ljúka eftirfarandi innan tilgreindra tímamarka:
Lýsing Tímamörk
- Til að ljúka lýsingu á eiginleikum virka efnisins og fullbúna lyfsins skal markaðsleyfishafi leggja fram viðbótargögn. Júlí 2021.
- Bráðabirgðaskýrslur: 31. mars 2021
- Til að tryggja samfelld gæði lyfsins skal markaðsleyfishafi veita viðbótarupplýsingar til að bæta eftirlitsaðferðina, þ.m.t. gæðalýsingu á virka efninu og fullbúna lyfinu í júlí 2021.
Til að staðfesta hreinleika og tryggja alhliða gæðaeftirlit og samræmi á milli lota á öllum framleiðslustigum (lifecycle) fullbúna lyfsins, skal markaðsleyfishafi veita frekari upplýsingar um framleiðsluferlið (synthetic process) og eftirlitsaðferð fyrir hjálparefnið ALC-0315. júlí 2021.
Bráðabirgðaskýrslur: Janúar 2021, apríl 2021
Til að staðfesta hreinleika og tryggja alhliða gæðaeftirlit og samræmi á milli lota á öllum framleiðslustigum fullbúna lyfsins, skal markaðsleyfishafi veita frekari upplýsingar um framleiðsluferlið og eftirlitsaðferð fyrir hjálparefnið ALC-0159. Júlí 2021.
Bráðabirgðaskýrslur: Janúar 2021, apríl 2021 og desember 2023
Lýsing

Tímamörk Til að staðfesta verkun og öryggi Comirnaty skal markaðsleyfishafi leggja fram lokaskýrslu klínískra rannsókna fyrir slembiröðuðu, blinduðu (observer blind) rannsóknina C4591001 með samanburði við lyfleysu.
- Þessi fylgiseðill var síðast uppfærður {MM/ÁÁÁÁ}
- Þetta lyf hefur fengið markaðsleyfi með svokölluðu „skilyrtu samþykki“ sbr. neyðarleyfi
- Það þýðir að beðið er frekari gagna um lyfið.
- Lyfjastofnun Evrópu metur nýjar upplýsingar um lyfið að minnsta kosti árlega og fylgiseðillinn verður uppfærður eftir því sem þörf krefur.
- Skannið kóðann með farsíma til að fá fylgiseðilinn á mismunandi tungumálum.
- Vefslóð: www.comirnatyglobal.com
- Ítarlegar upplýsingar um lyfið eru birtar á vef Lyfjastofnunar Evrópu http://www.ema.europa.eu.
Þessi fylgiseðill er birtur á vef Lyfjastofnunar Evrópu á tungumálum allra ríkja Evrópska efnahagssvæðisins.
Um höfund

- Sigurlaug Ragnarsdóttir
- ✞༺(((( Ⓒilla ℜągnąℜṧ )))༻♚༺ BA Classical Art Historian || MA Culture & Media || Tourism & Sales Management || Web Design || Photo & Videographer for Tourism Magasins ༻
Síðustu færslur
 PROTECT THE CHILDREN23. nóvember, 2024BARNAMÁLARÁÐSTEFNAN 2024
PROTECT THE CHILDREN23. nóvember, 2024BARNAMÁLARÁÐSTEFNAN 2024 MANNRÉTTINDI19. nóvember, 2024MENNTASPJALL VALGERÐAR SNÆLAND JÓNSDÓTTUR
MANNRÉTTINDI19. nóvember, 2024MENNTASPJALL VALGERÐAR SNÆLAND JÓNSDÓTTUR MANNRÉTTINDI9. ágúst, 2024Lög um borgaralega handtöku voru felld úr gildi árið 2008
MANNRÉTTINDI9. ágúst, 2024Lög um borgaralega handtöku voru felld úr gildi árið 2008 Sameinuðu Þjóðirnar28. desember, 2023Lestrarefni Menntamálastofnunar: Varúð hér býr vampíra – auðlesin sögubók á léttu máli og bókinni fylgir verkefnahefti sem hægt er að vinna samhliða lestri.
Sameinuðu Þjóðirnar28. desember, 2023Lestrarefni Menntamálastofnunar: Varúð hér býr vampíra – auðlesin sögubók á léttu máli og bókinni fylgir verkefnahefti sem hægt er að vinna samhliða lestri.